根据观研报告网发布的《2021年中国生物医药市场分析报告-产业竞争现状与发展前景预测》显示,近年来国家相关部门相继出台多项政策,对医药行业进行了鼓励创新改革,涉及的方面包括减少新药注册审评流程、加快创新药审评审批、减免进口药物关税、国家谈判进医保促进销量增长等,对生物医药行业发展有着长足的促进作用。
| 发布时间 |
政策名称 |
主要内容 |
| 2021年3月 |
《国家免疫规划疫苗儿童免疫程序及说明(2021年版)》 |
新版程序及说明主要有两大变化,是优化调整
部分接种程序和剂型,二是对长期困扰基层医疗工作者、临床医生和家长的常见特殊健康状态儿童接种问题进行了说明。 |
| 2021年3月 |
《“十四五”生物医药产业发展规划》 |
推动生物技术和信息技术融合创新,加快发展生物医药等产业,做大做强生物经济:聚焦生物医药等重大创新领城组建-批国家实验室,重组国家重点实验室,形成结构合理、运行高效的实验家体系。 |
| 2021年2月 |
《疫菌生产流通管理规定(征求意见稿)》 |
国家约监局维织起草了该意见。目的在于构建科学,有效的疫菌生产流通监督管理体系,依法对疫苗的生产,流通管理活动进行规范。 |
| 2020年12月 |
《生物制品批签发管理办法( 2020修订版)》 |
从申请、检验、审核与签发、复事、监督与处罚等方面对生物制品批签发制度做了规定。 |
| 2020年11月 |
《粤港澳大湾区药品医疗器械监管创新发展工作方案》 |
粤港澳三地生物医药产业创新要素和产业布局齐全,拥有一批具有影响力的高等院校、科研机构和生物医药企业, 形成了以香港、澳门联通全球的生物医药产业格局,创新发展、集聚发展和跨越发展基础优势显著。 |
| 2020年7月 |
关于发布《突破性治疗药物审评工作程序(试行)》等三个文件的公告(2020年第82号) |
为配合《药品注册管理办法》实施,国家药品监督管理局组织制定了《突破性治疗药物审评工作程序(试行)》《药品附条件批准上市申请审评审批工作程序(试行)》《药品上市许可优先审评审批工作程序(试行)》 |
| 2020年7月 |
《药品注册管理办法》 |
规定了药品上市注册的程序、加快上市注册程序、上市后变更和再注册、受理、撤回申请、审批决定和争议解决等。 |
| 2020年4月 |
《药物临床试验质量管理规范》 |
对药物临床试验全过程的标准进行规定,包括方案设计、组织实施、监查、稽查、记录、分析总结和报告等。。 |
| 2020年3月 |
《药品生产监督管理办法》 |
加强药品生产的监督管理,规范药品生产活动和风险处置;明确上市许可持有人取得《药品生产许可证》,对药品生产质量管理规范符合性检查明确规定等。 |
| 2020年3月 |
《药品注册管理办法》 |
规范药品注册行为,保证药品的安全、有效和质量可控;加强从药品研制上市、上市后管理到药品注册证书注销等各环节全过程、全链条的监管制度。 |
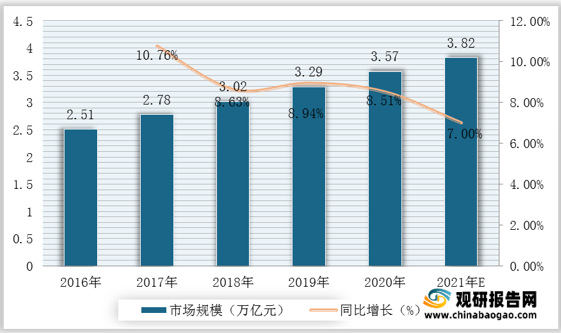
近年来,随着国家对生物医药行业的高度重视,我国医药企业发展整体趋势由快速增长到趋于稳定。2019年我国规模以上生物医药企业实现主营业务收入2479.2亿元,2020年我国规模以上生物医药企业实现主营业务收入约为2727.1亿元,同比增长10%。


| 趋势 |
主要内容 |
| 海洋药物成为科技研发热点 |
目前,现代化的海洋制药生产企业遍布沿海各省市。在山东,国风、华仁、博新生物等生物医药企业与高校、科研机构组成的海洋药物和保健品研究开发产业体系已经成形。未来10余年中国将形成一批海洋药物与保健品, 并在抗艾滋病、抗肿瘤、卫生保健方面发挥重要作用。 |
| 抗体基因成市场主流 |
随着免疫学和分子生物学技术的发展以及抗体基因结构的闸明,DNA重组技术开始用于抗体的改造,抗体药物目前已经进入基因工程抗体时代。抗体药物是近年来复合增长率最快的一类生物技 术药物。 |
行业分析报告是决策者了解行业信息、掌握行业现状、判断行业趋势的重要参考依据。随着国内外经济形势调整,未来我国各行业的发展都将进入新阶段,决策和判断也需要更加谨慎。在信息时代中谁掌握更多的行业信息,谁将在未来竞争和发展中处于更有利的位置。


【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。